ETH-Forschende haben einen Genschalter entwickelt, der sich mit dem grünen LED-Licht handelsüblicher Smartwatches betätigen lässt – eine Premiere, die künftig für die Diabetesbehandlung genutzt werden könnte.
Viele moderne Sportuhren oder Smartwatches haben LED-Dioden integriert. Diese geben kontinuierlich oder gepulst grünes Licht ab, das die Haut durchdringt und unter anderem dafür genutzt wird, während sportlicher Betätigung oder in Ruhe den Puls zu messen.
Solche Uhren sind mittlerweile weit verbreitet. Darum wollen ETH-Forschende um Martin Fussenegger vom Departement Biosysteme in Basel diese Lichtquelle nutzen, um durch die Haut hindurch Gene zu steuern und das Verhalten von Zellen zu verändern. Die Schwierigkeit dabei: „Ein molekulares System, das auf Grünlicht reagiert, gibt es natürlicherweise in menschlichen Zellen nicht“, betont Fussenegger, „wir mussten deshalb etwas Neues konstruieren.“
Grünlicht der Uhr aktiviert Gen
Entwickelt haben der ETH-Professor und seine Mitarbeitenden schliesslich einen molekularen Schalter, der – einmal implantiert – mit grünem Licht von Smartwatches aktiviert werden kann.
Der Schalter ist gekoppelt mit einem genetischen Netzwerk, das die Forschenden menschlichen Zellen hinzufügten. Für diesen Prototyp verwendeten sie wie üblich HEK-Zellen. Je nach Konfiguration dieses Netzwerks – sprich: mit welchen Genen es ausgestattet ist – kann es beispielsweise Insulin produzieren, sobald grünes Licht auf die Zellen trifft. Wird das Licht ausgeschaltet, wird der Schalter inaktiviert und der Vorgang stoppt.
Standardsoftware von Smartwatches genutzt
Die Forschenden benutzten dafür die Standardsoftware der Smartwatch und mussten nicht einmal eigene Programme entwickeln. In ihren Versuchen konnten sie das Grünlicht einschalten, indem sie die „Lauf-App“ starteten.
„Solche Uhren ab Stange sind universell nutzbar, um den molekularen Schalter umzulegen“, sagt Fussenegger. Neue Modelle senden das Licht gepulst, was sich noch besser eignet, um das Gennetzwerk am Laufen zu halten.
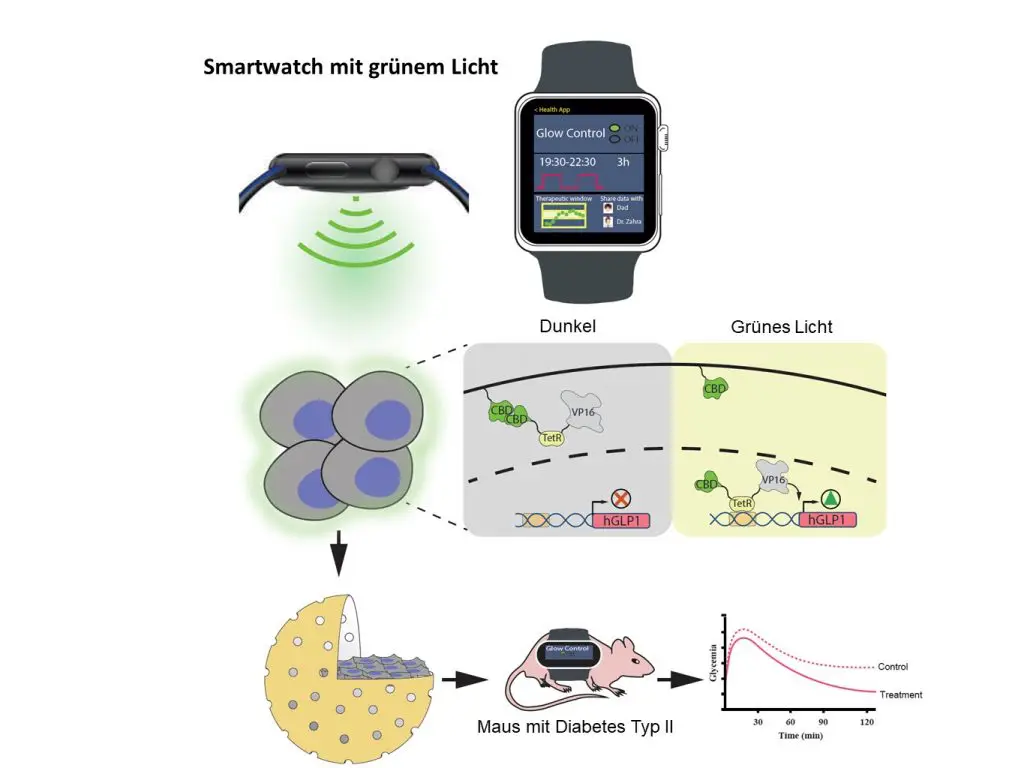
Der molekulare Schalter ist allerdings komplizierter. In der Membran der HEK-Zellen wurde ein Molekülkomplex eingebaut, der ähnlich einer Eisenbahnwagenkupplung mit einem entsprechenden Gegenstück gekoppelt ist. Sobald grünes Licht angeschaltet wird, löst sich das in das Zellinnere hineinragende Stück ab und wird in den Zellkern transportiert. Dort schaltet es ein Gen an, das Insulin produziert. Sobald das Grünlicht erlischt, verbindet sich das abgekoppelte Teil wieder mit dem in der Membran verankerten Gegenstück.
Implantat mit Wearables steuern
Ihr System testeten die Forschenden sowohl an einer Speckschwarte als auch an lebenden Mäusen, denen sie die entsprechenden Zellen implantierten und eine Smartwatch wie ein Rucksack anschnallten. Durch das Starten des Laufprogramms der Uhr schalteten die Forschenden das Grünlicht ein und setzten die Kaskade in Gang.
„Es ist das erste Mal, dass man mit kommerziell erhältlichen intelligenten elektronischen Geräten, die auf der Hautoberfläche getragen werden, sogenannten Wearables, ein solches Implantat steuern kann“, betont der ETH-Professor. Die meisten Uhren verfügen über grünes Licht, weshalb es sinnvoll ist, eine mögliche künftige Anwendung darauf auszurichten. Auf diese Weise müssten Anwenderinnen und Anwender kein spezielles Gerät kaufen.
Bis die Technologie in die Klinik kommt, würde es allerdings mindestens 10 Jahre brauchen, schätzt Fussenegger. Die in diesem Prototyp verwendeten Zellen müssten durch Eigenzellen des Anwenders ersetzt werden; auch muss das System die klinischen Phasen überstehen, ehe es zugelassen wird. Die Hürden dafür sind hoch: „Bis heute gibt es nur sehr wenige zugelassene Zelltherapien“, betont Fussenegger.
